Адсорбция органических реагентов природным бентонитом, модифицированным полигидроксокомплексами алюминия и железа (III)
Получены эффективные наноструктурные сорбенты на основе природного бентонита, модифицированного полигидроксокатионами алюминия и железа(III). Изучен элементный состав полученных сорбентов.
Известия Саратовского университета. Новая серия.
Серия: Химия. Биология. Экология. 2021. Т. 21, вып. 1. С. 23–30
Izvestiya of Saratov University. New Series.
Series: Chemistry. Biology. Ecology, 2021, vol. 21, iss. 1, pp. 23–30
https://ichbe.sgu.ru/ru/journal/2021/1
Научная статья
УДК 541.183
Адсорбция органических реагентов природным бентонитом, модифицированным
полигидроксокомплексами алюминия и железа (III)
Нат. В. Никитина, А. П. Ламихова, Над. В. Никитина, И. А. Казаринов
Саратовский национальный исследовательский государственный университет имени Н. Г. Чернышевского, Институт химии, Россия, 410012, г. Саратов, ул. Астраханская, д. 83
ООО «Научно-исследовательский институт технологий органической, неорганической химии и биотехнологий» (ООО «НИИТОНХ и БТ»), Россия, 410005, г. Саратов, ул. Большая Садовая, д. 239Л
Adsorption of organic reagents by natural bentonites modified with aluminum and iron (III) polyhydroxocations
Natalya V. Nikitina, Anna P. Lamikhova, Nadezhda V. Nikitina, Ivan A. Kazarinov
Saratov State University, 83 Astrakhanskaya St., Saratov 410012, Russia
LLC “Scientific research Institute technology organic, inorganic chemistry and biotechnologies” ,
239L Bolshaya Sadovaya St., Saratov 410005, Russia
Аннотация. Получены эффективные наноструктурные сорбенты на основе природного бентонита, модифицированного полигидроксокатионами алюминия и железа(III). Изучен элементный состав полученных сорбентов. Для исследуемых образцов сорбентов была определена площадь удельной поверхности. Показано, что модифицированные сорбенты на основе природного бентонита являются наноструктурными объектами. Методом ИК-спектроскопии установлено, что модифицирование природного бентонита приводит к изменению его структурных свойств. При изучении сорбционного процесса на модифицированных сорбентах установлено, что модифицирование бентонита соединениями алюминия и железа(III) методом «соосаждения» приводит к увеличению сорбционной ёмкости полученных сорбентов. Сорбционные свойства полученных сорбентов проверяли по отношению к ряду органических красителей анионного и катионного типа. Установлено, что максимальная эффективность сорбции достигается для извлечения из воды веществ катионного типа, в том числе и органических красителей.
Ключевые слова: бентонит, сорбция, сорбция органических реагентов, полигидроксокатионы, наноструктурные сорбенты
Abstract. The effective nanostructured sorbents based on natural bentonite modified with aluminum and iron (III) polyhydroxocations were obtained. The elemental composition of the obtained sorbents was studied. The specific surface area was determined for the studied samples. It was shown that modified sorbents based on natural bentonite were nanostructured objects. IR spectroscopy showed that modification of natural bentonite led to the changes in its structural properties. While studying the sorption process on modified sorbents, it was found that the modification of bentonite with aluminum and iron (III) compounds using the “codeposition” method led to the increase in the sorption capacity of the obtained sorbents. The sorption properties of the obtained sorbents were tested in relation to a number of organic dyes of the anionic and cationic types. It was established that the maximum sorption efficiency was achieved for extracting cationic substances from water, including organic dyes.
Keywords: bentonite, sorption, sorption of organic reagents, polyhydroxocations
Введение
Природные глинистые материалы успешно используются в качестве сорбентов как неорганических, так и органических соединений благодаря большому числу активных кислотных и основных центров на поверхности глины. Одним из преимуществ глинистых минералов является то, что их структура позволяет провести целенаправленное модифицирование с целью регулирования поверхностных свойств и адсорбционных характеристик.
Повышение адсорбционных характеристик природных алюмосиликатов возможно путём ионного обмена, обработкой их кислотами, щелочами и солями различных металлов, которые приводят к увеличению концентрации кислотных и основных центров, изменению энергии переноса заряда, облегчению электронных переходов и подвижности ионов.
С практической точки зрения среди глинистых минералов особое место занимает бентонит, модифицированные образцы которого находят широкое применение при очистке сточных вод от химических загрязнений неорганической и органической природы [1]. При сравнении адсорбционной активности по отношению к органическим соединениям бентонитовые глины имеют преимущество перед цеолитами из-за большого межплоскостного расстояния, куда легко проникают длинноцепочечные органические соединения.
Целью настоящей работы является изучение физико-химических характеристик и сорбционной способности модифицированных полигидроксокатионами алюминия и железа(III) сорбентов на основе бентонита по отношению к органическим реагентам.
Материалы и методы
В работе был использован природный бентонит Саригюхского месторождения (Иждеванский район, Республика Армения) и его Fe(III)- и Al- модифицированные формы. Бентонит был модифицирован полигидроксокатионами железа(III) и алюминия методом «соосаждения». Образцы были гранулированы методом вихревой накатки и отожжены при температуре 550° С в инертной атмосфере аргона [2].
Количественный анализ элементного состава производился на энергодисперсионном рентгеновском флуоресцентном спектрометре EDX–720 (SHIMADZU, Япония) методом фундаментальных параметров.
Пористую структуру образцов определяли по низкотемпературной адсорбции азота на быстродействующем анализаторе сорбции газов Quantachrome NOVA (США). Для измерения удельной поверхности твёрдых образцов использовался метод Брунауэра–Эммета–Тейлора (БЭТ). Для измерения объёма пор и определения распределения пор по размерам использовался метод Barrett-Joyner-Halenda (BJH). Химический состав природного бентонита, а также модифицированных сорбентов на его основе был изучен методом инфракрасной спектроскопии. ИК-спектры снимали на ИК-фурье-спектрометре ФСМ-1201.
Для изучения сорбционной способности модифицированных сорбентов готовили исходные растворы красителей «метиленовый голубой», относящийся к классу хинониминовых красителей, «конго красный», относящийся к классу диазокрасителей, «кислотный хром тёмно-синий», «эриохром чёрный Т», «метиленовый оранжевый», относящиеся к классу азокрасителей, «крезоловый красный», относящийся к классу трифенилметановых красителей. Для построения градуировочного графика готовили растворы красителей с концентрациями 1.0; 2.5; 5.0; 7.5; 10.0 мг/л из исходного раствора с концентрацией 100 мг/л [3]. Значения оптической плотности растворов снимали на спектрофотометре КФК–3 относительно дистиллированной воды. Строили графики зависимости оптической плотности от концентрации красителя Скрасителя. Содержание красителя в водной фазе определяли спектрофотометрически по градуировочному графику с использованием спектрофотометра при соответствующих длинах волн λ: метиленовый голубой – 668 нм, метиленовый оранжевый – 464 нм, конго красный – 505 нм, кислотный хром тёмно-синий – 550 нм, крезоловый красный – 434 нм, эриохром чёрный Т – 525 нм [4].
По средним значениям равновесных концентраций (не менее двух параллельных измерений) величину адсорбции рассчитывали по следующей формуле (1):
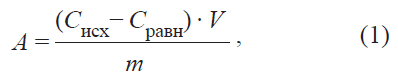
где A – адсорбция, мг/г; Cисх – исходная концентрация исследуемых ионов в растворе, мг/л; Cравн – равновесная концентрация исследуемых ионов в растворе, мг/л; V – объём исследуемого раствора, л; m – масса сорбента, взятого для анализа, г.
Объекты исследования:
– образец 1 – исходный порошок природногобентонита;
– образец 1-ГО – исходный порошок природного бентонита, гранулированный методом вихревой накатки и отожжённый при 550ºС в инертной атмосфере аргона;
– образец Fe-МБГО – исходный порошок природного бентонита, модифицированный полигидроксокатионами железа(III) по методу «соосаждения», гранулированный методом вихревой накатки и отожжённый при температуре 550ºС в инертной атмосфере аргона;
– образец Al-МБГО, исходный порошок природного бентонита, модифицированный полигидроксокатионами алюминия по методу «соосаждения», гранулированный методом вихревой накатки и отожжённый при температуре 550ºС в инертной атмосфере аргона.
Результаты и их обсуждение
Элементный состав исследуемых сорбентов
Анализ элементного состава исследуемых сорбентов показал, что основными элементами в образцах сорбентов являются кремний и алюминий с примесями железа, кальция, калия, титана и циркония (табл. 1). Модифицирование бентонита полигидроксокатионами Al3+ и Fe3+ приводит к повышению концентрации соответствующего элемента в образце бентонита. Это повышение происходит в результате замещения обменных катионов глины.
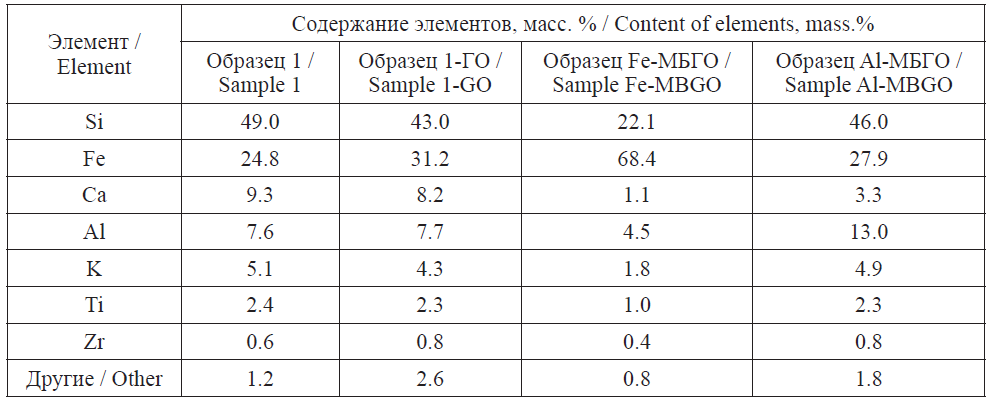
Элементный состав исследуемых сорбентов
The elemental composition of the studied sorbents
Пористая структура модифицированных сорбентов
Модифицирование бентонита полигидроксокатионами железа(III) и алюминия приводит к увеличению площади удельной поверхности за счёт образования первичных щелевидных микропор и формирования слоистой столбчатой структуры [5] (табл. 2).
Из данных табл. 2 видно, что модифицирование бентонита приводит к уменьшению числа макропор (>8 нм) и увеличению числа микро- и мезопор (1.5–4.0 нм), в сравнении с исходным бентонитом. Большая часть пор всех модифицированных образцов приходится на поры размером 1.5–8.0 нм [2, 6].
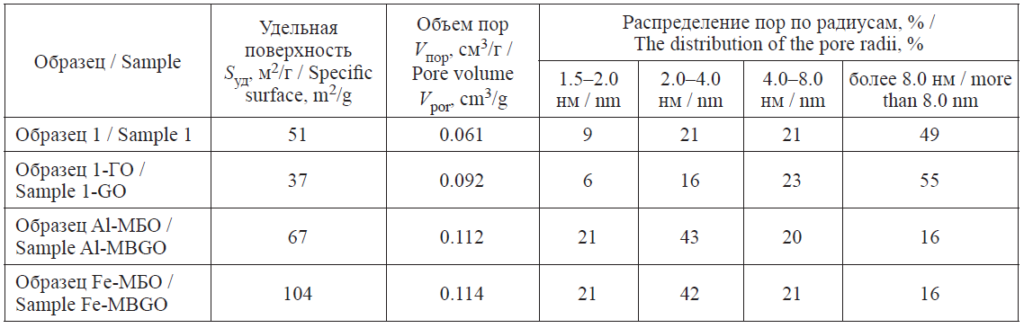
Основные характеристики пористой структуры модифицированных сорбентов на основе бентонита
The basic characteristics of the porous structure of modifi ed sorbents based on bentonite
ИК-спектральный анализ
ИК-спектры образцов отражают набор полос поглощения, характерный для структуры монтмориллонита (рис. 1) [7].
В области 4000–3000 см-1 расположены полосы валентных колебаний ОН-групп, связанные с октаэдрическими катионами, а также молекул воды, во второй области 1400–400 см-1 расположены полосы силикатной структуры [8, 9].
ИК-спектры содержат характерные для основной фазы монтмориллонита полосы в области валентных и деформационных колебаний структурных групп, а также полосы явно характерных примесей – коалинита и α-кварца. Результаты идентификации ИК-спектров всех образцов сорбентов обобщены в табл. 3. Спектры указывают на то, что образцы являются полифазными.
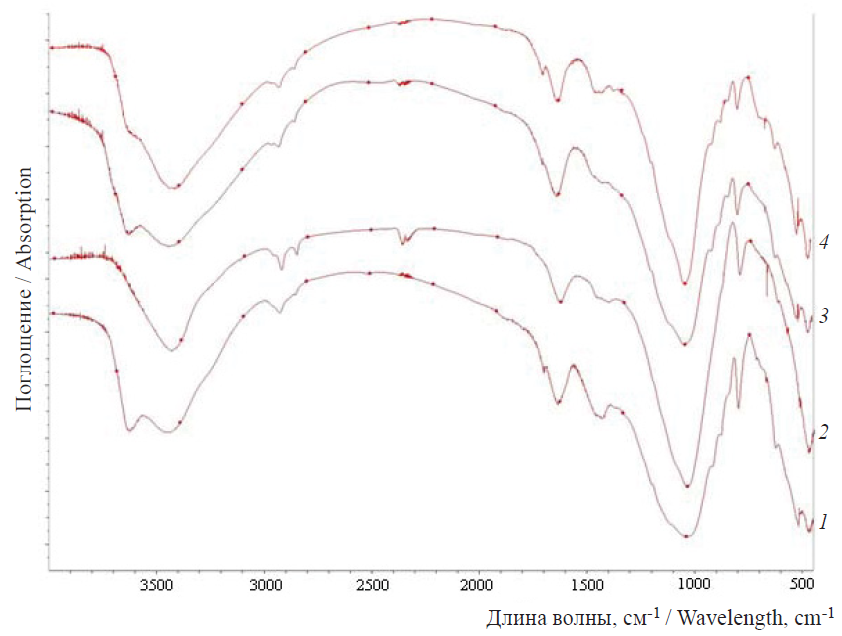
Fig. 1. The IR spectra of the studied sorbents: 1 – sample 1, 2 – sample 1-GO, 3 – sample Al-MBGO, 4 – sample Fe-MBGO
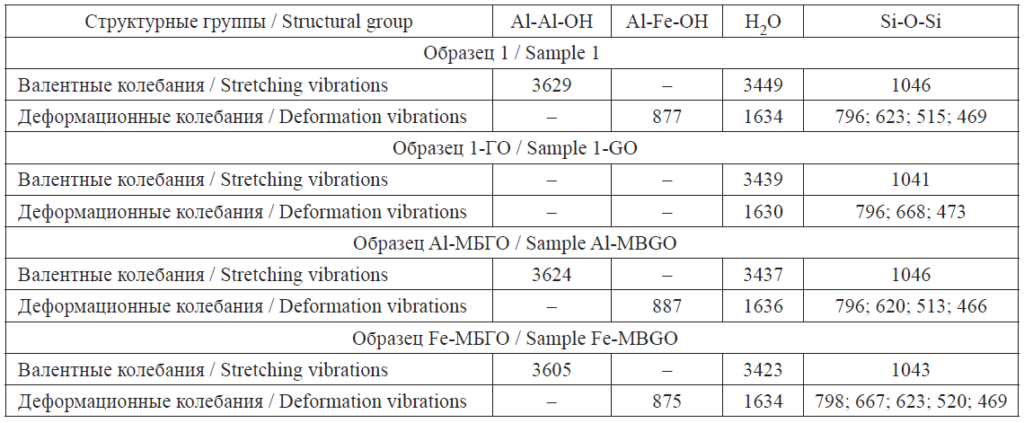
Волновые числа (ν, см-1) максимумов поглощения в ИК-спектрах исследуемых образцов сорбентов
The wave numbers (ν, cm-1) of the absorption maxima in the IR spectra of the studied sorbent samples
Изучение сорбционной способности модифицированных сорбентов
Навески исследуемых образцов сорбентов массой 2 г заливали дистиллированной водой на 1 ч, затем декантировали и заливали 100 мл модельного раствора (крезоловый красный, метиленовый голубой, конго красный, кислотный хром тёмно-синий, метиленовый оранжевый, эриохром чёрный Т) различной концентрации, выдерживали 2 ч до достижения равновесной концентрации в растворе. Затем отбирали пробы из средних слоёв раствора. Данные по кинетике сорбции этих органических реагентов на исследуемых сорбентах приведены на примере раствора крезоловый красный, метиленовый голубой, конго красный, метиленовый оранжевый (рис. 2–5).
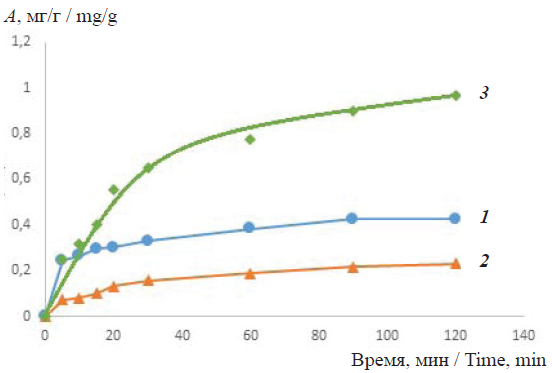
Fig. 2. The kinetic adsorption curves from a solution of cresol red in a neutral medium on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO
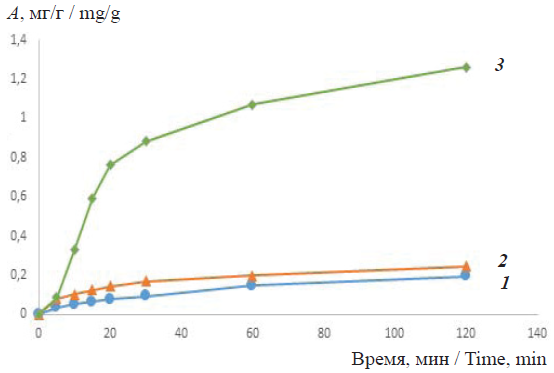
Fig. 3. The kinetic adsorption curves from a solution of methylene blue in a neutral medium on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO
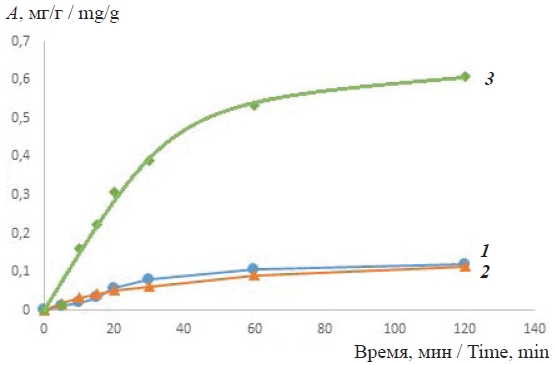
Fig. 4. The kinetic absorption curves from the Congo-red solution in a neutral medium on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO
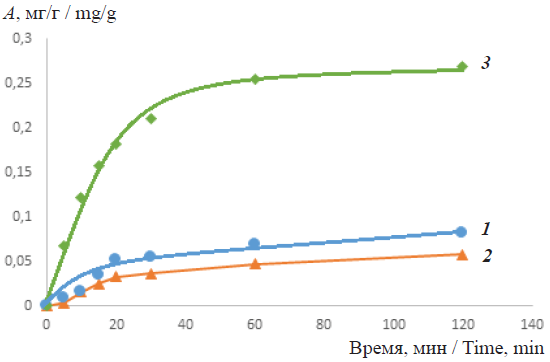
Fig. 5. The kinetic absorption curves from a solution of methylene orange in a neutral medium on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO
На рис. 6–9 (а) представлены изотермы сорбции органических красителей на исследуемых сорбентах. Полученные изотермы аппроксимируются уравнением типа Ленгмюра. Уравнение изотермы сорбции Ленгмюра, выведенное на основе молекулярно-кинетической теории и представлений о мономолекулярном характере процесса сорбции, имеет вид (2):
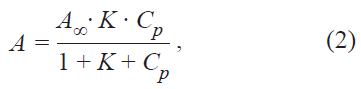
где А∞ – предельная мономолекулярная адсорбция, мг/г; Ср – равновесная концентрация, мг/л; K – константа адсорбционного равновесия, л/моль.
Изотерма сорбции Ленгмюра линеаризуется в координатах A-1, C-1 (3), что позволяет графоаналитически определить значения коэффициентовК и А∞.
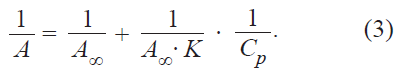
Обработка полученных изотерм сорбции в соответствии с уравнением Ленгмюра в обратных координатах (3) представлена на рис. 6–9 (б).
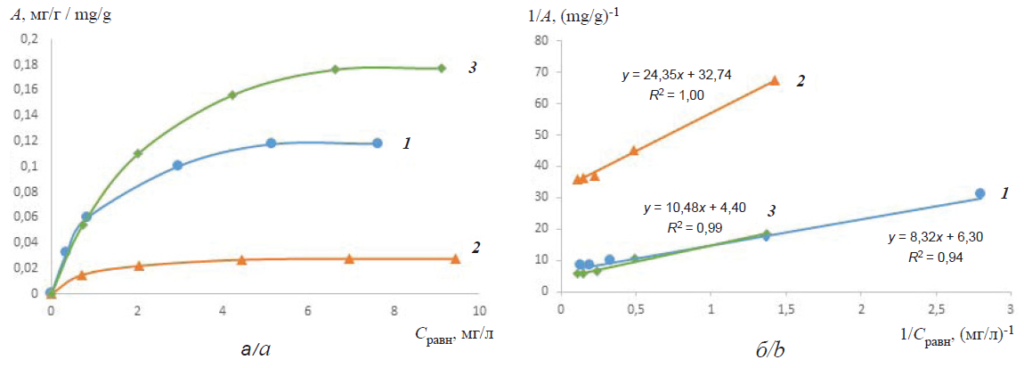
Fig. 6. Isotherms of adsorption of cresol red in a neutral medium from a solution on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (a); isotherms of sorption of cresol red in a neutral medium from a solution, represented in inverse coordinates in accordance with the Langmuir equation, on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (b)
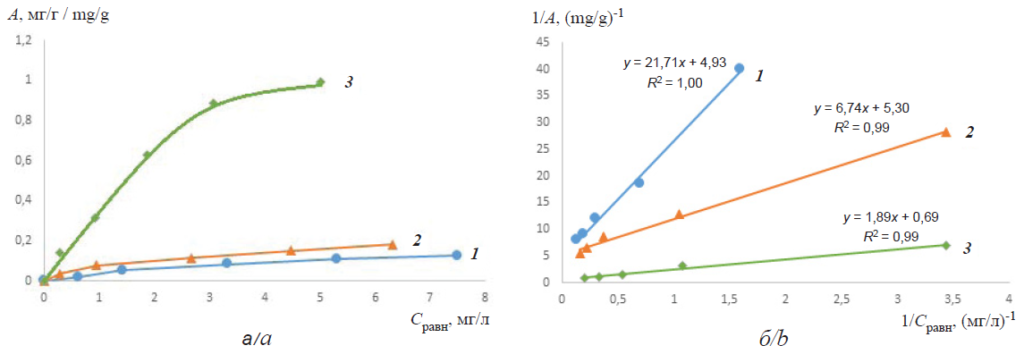
Fig. 7. Isotherms of adsorption of methylene blue in a neutral medium from a solution on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (a); isotherms of sorption of methylene blue in a neutral medium from a solution, represented in inverse coordinates in accordance with the Langmuir equation, on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (b)
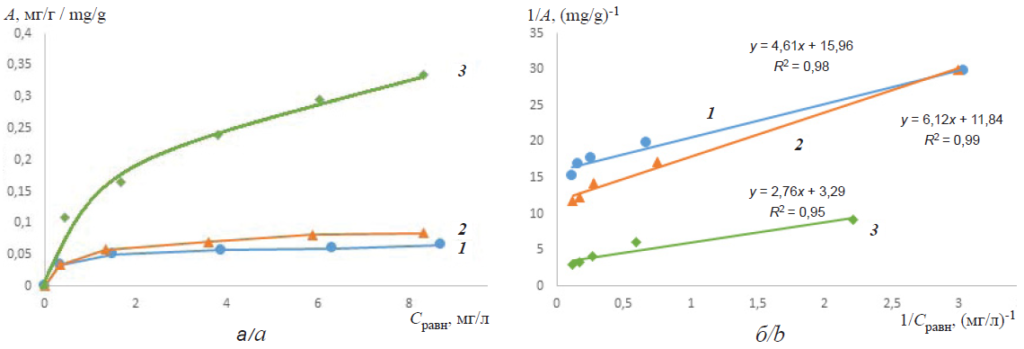
Fig. 8. Isotherms of adsorption of Congo-red in a neutral medium from a solution on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (a); isotherms of sorption of Congo-red in a neutral medium from a solution, represented in inverse coordinates in accordance with the Langmuir equation, on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (b)
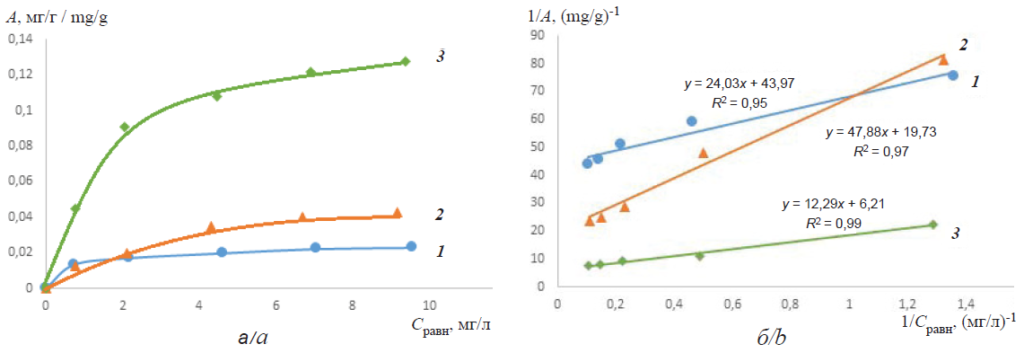
Fig. 9. Isotherms of adsorption of methylene orange in a neutral medium from a solution on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (a); isotherms of sorption of methylene orange in a neutral medium from a solution, represented in inverse coordinates in accordance with the Langmuir equation, on sorbents: 1 – 1-GO, 2 – Fe-MBGO and 3 – Al-MBGO (b)
Обработка полученных изотерм сорбции позволила оценить величину предельной сорбционной ёмкости исследуемых сорбентов по отношению к исследуемым органическим реагентам. В табл. 4 приведена величина предельной адсорбции органических соединений на исследуемых сорбентах.
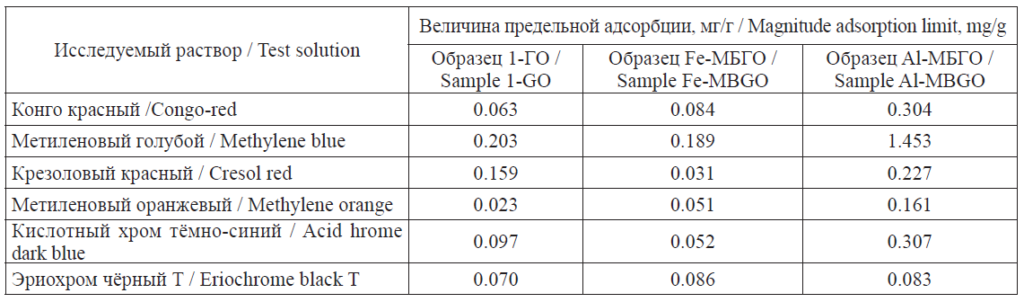
Значения величин предельной адсорбции для органических соединений на исследуемых сорбентах
The values of the maximum adsorption for organic compounds on the studied sorbents
Термообработка модифицированных бентонитов приводит к образованию жесткой слоисто-столбчатой структуры с наличием щелевидных микропор, которые недоступны для адсорбции крупных ассоциатов многих органических красителей. Поскольку при модифицировании глин полигидроксокатионами алюминия и железа(III) изменяется знак заряда поверхности, то наибольшая величина предельной адсорбции наблюдается для органических реагентов катионного типа (метиленовый голубой). Использование модифицированных бентонитов при очистке сточных вод от анионных красителей (конго красный, кислотный хром тёмно-синий, эриохром чёрный Т, метиленовый оранжевый, крезоловый красный) является менее эффективным, поскольку органические анионы адсорбируются только на положительно заряженных боковых гранях бентонитов. Следует отметить, что наибольшую сорбционную активность проявляют Al-модифицированные образцы сорбентов.
Заключение
Изучены физико-химические и сорбционные свойства природного бентонита и модифицированных сорбентов на его основе. Установлено, что модифицирование бентонита полигидроксокатионами железа и алюминия приводит к изменению их химического состава и сорбционных свойств. Происходит увеличение общей площади удельной поверхности (до 104 м2/г), что объясняет повышение сорбции анионов и катионов на модифицированных сорбентах.
Установлено, что величина предельной адсорбции образцов, модифицированных полигидроксокатионами, зависит от природы исследуемых органических реагентов. Наибольшая величина предельной адсорбции наблюдается для органических реагентов катионного типа.
Список литературы
1. Ягубов А. И. Сорбционные процессы очистки сточных вод от метилена голубого на Fe(III) бентоните :
экспериментальные исследования и моделирование //Конденсированные среды и межфазные границы. 2007.
Т. 9, № 2. С. 177–181.
2. Никитина Нат. В., Комов Д. Н., Казаринов И. А., Никитина Над. В. Физико-химические свойства сорбентов
на основе бентонитовых глин, модифицированных полигидроксокатионами железа (III) и алюминия методом «соосаждения» // Сорбционные и хроматографические процессы. 2016. Т. 16, № 2. С. 191–199.
3. Kloprogge J. T. Synthesis of Smectites and Porous Pillared Clay Catalyst: Review // J. of Porous Materials. 1998. Vol. 5. P. 5–41.
4. Комаров B.C. Адсорбенты. Вопросы теории синтеза и структуры. Минск : Беларуская навука, 1997. 287 с.
5. Khankhasaeva S. Ts., Badmaeva S. V., Dashinamzhilova E. Ts., Bryzgalova L. V., Ryazantsev A. A. Adsorption of Anionic Dyes on Montmorillonite Modifi ed with Polyhydroxo Complexes of Aluminium and Iron // Chemistry for Sustainable Development. 2006. Vol. 14. P. 287–294.
6. Никитина Над. В., Казаринов И. А., Никитина Нат. В. Физико-химические свойства сорбентов на основе природного бентонита // V Междунар. конференция-школа по химической технологии ХТ’16 : сб. тез. докл.
сателлит. конф. XX Менделеевского съезда по общей и прикладной химии : в 3 т. Волгоград : ВолгГТУ, 2016.
Т. 3. С. 315–317.
7. Тарасевич Ю. И. Строение и химия поверхности слоистых силикатов. Киев : Наук. думка, 1988. 248 с.
8. Ракитская Т. Л., Киосе Т. А., Джига А. М., Топоров С. В. ИК-спектральное исследование структуры и фазового состава бентонитов Украины // Вісник ОНУ. Хімія. 2012. Т. 17, № 1. С. 13–19.
9. Вакалова Т. В. Глины. Особенности структуры и методы исследования. Томск : ТГУ, 1998. 121 с.